Методология флоуметрии, Âûïóñê 6, 2002 ã. стр.107-117.
Исследование нейрогенных вазоконстрикторных ответов у наркотизированных крыс
В.О. Голубинская1, О.С. Тарасова2, А.С. Боровик1, О.Л. Виноградова1
1Учебно-Исследовательский
Центр Космической Биомедицины,
2Биологический факультет МГУ им. М.В. Ломоносова, Москва
Нейрогенные механизмы регуляции сосудистой системы являются важнейшим элементом адаптации организма к изменяющимся условиям окружающей среды. Для понимания возможностей адаптации необходимы исследования регуляции сердечно-сосудистой системы, и в частности действие симпатической нервной системы на различные сосудистые бассейны. Такие исследования можно проводить на разных уровнях – от изучения условий формирования центральной команды до выявления механизмов ее реализации на периферии, т.е. на уровне сосудистого бассейна или даже одиночного сосуда. Несомненно, наиболее приближенными к естественным являются условия бодрствующего организма, однако в этом случае одновременная работа и сложное взаимодействие регуляторных систем затрудняют анализ механизмов наблюдаемых явлений. Эксперименты, проводимые на изолированных сосудах, проще анализировать, но вся система при этом сильно упрощена и удалена от реальных условий. Описанный в этой статье метод изучения in vivo регуляции сосудистого сопротивления в различных органах у наркотизированных крыс позволяет сопоставить результаты таких исследований.
Материалы и методы исследования
В опытах использовали крыс линии Вистар весом 300-400 г. Животных наркотизировали уретаном (1,5 г/кг, внутрибрюшинно). Дозу вещества вводили двумя порциями: сначала 1 г/кг, а через полчаса, перед началом препаровки - остальное.
Крысу располагали на термостатируемом (37°С) столике брюшной стороной вверх. В течение эксперимента крыса дышала спонтанно через трахеотомическую трубку. Веточку бедренного нерва, идущую вдоль подкожной артерии, выделяли, перевязывали и перерезали дистально от лигатуры. После срединной лапаротомии отсепаровывали левую общую подвздошную и левую почечную артерии и подводили под них лигатуры. Регистрацию объемной скорости кровотока проводили сначала в подвздошной артерии, а затем – в почечной с помощью датчика 1RB и флоуметра Transonic Systems Inc., модель T106. Для измерения артериального давления через бедренную артерию вставляли катетер таким образом, чтобы его кончик находился на том же уровне, где замерялся кровоток в левой подвздошной артерии или в брюшной аорте в области почечной артерии. Экспериментальные данные регистрировали и анализировали с помощью прецизионного АЦП (L-Card, Москва) и оригинального программного обеспечения. Частота оцифровки данных составляла 200 Гц.
Исследовали реакции сосудов при сосудодвигательных рефлексах (в ответ на пережатие общей сонной артерии и на раздражение соматических афферентов), а также при раздражении эфферентных симпатических нервов.
Для того, чтобы рефлекторные сосудистые ответы не маскировались рефлекторными изменениями сердечного ритма, блуждающие нервы перерезали в области шеи. Одну сонную артерию перевязывали, вторую пережимали на 30 секунд с помощью миниатюрного зажима из стальной проволоки. Афферентные нервные волокна, проходящие в составе веточки бедренного нерва, расположенной вдоль подкожной артерии, раздражали с помощью биполярных серебряных электродов прямоугольными электрическими импульсами, которые поступали от стимулятора ЭСЛ-2 через изолирующий трансформатор. Параметры импульсов были следующими: амплитуда –15 В, длительность – 1 мс, частота – 10 Гц; длительность раздражения составляла 30 с.
Раздражение эфферентных симпатических волокон проводили только для сосудистого бассейна задней конечности. На уровне поясничного отдела под левую симпатическую цепочку подводили биполярные серебряные электроды. Выше электродов цепочку перевязывали. Раздражение проводили так же, как и для бедренного нерва, частота следования импульсов составляла 5, 10, 15 и 20 Гц, раздражение длилось 20 с. После каждого воздействия в течение примерно 5 мин дожидались восстановления регистрируемых параметров.
Проводили поударную обработку данных: для каждого сердечного цикла вычисляли среднее значение артериального давления, объемной скорости кровотока и длительность этого цикла. Величину констрикторного ответа при воздействиях оценивали по изменению гидравлического сопротивления сосудистого бассейна: R=P/Q, где R – сопротивление, P – артериальное давление, Q – объемная скорость кровотока.
А
Б
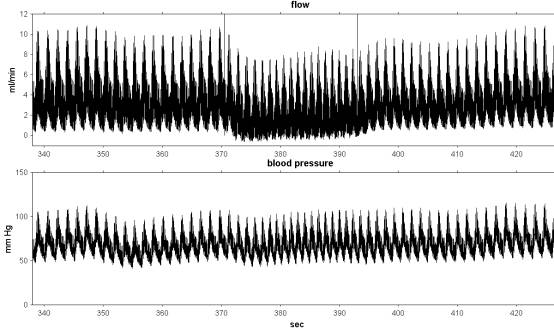
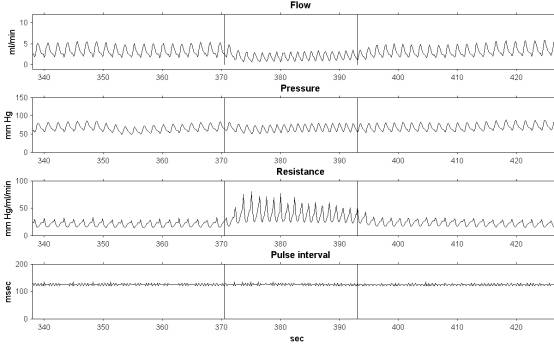
Рисунок 10.1. Примеры регистрации кровотока и артериального давления в подвздошной артерии при электрической стимуляции симпатических эфферентов с частотой 10 Гц. Представлены оригинальные кривые (А) и результат поударной обработки, т.е кривые среднего кровотока, среднего артериального давления, регионарного сопротивления и пульсового интервала (Б). Метки указывают начало и конец стимуляции.
Результаты
В ходе эксперимента в течение достаточно длительного времени одновременно регистрировались кровоток и артериальное давление в фоне и при сосудодвигательных реакциях. На рис. 10.1А представлен пример экспериментальной записи, во время которой проводилась электрическая стимуляция (частота импульсов 10 Гц) симпатических эфферентов. Видно, что кровоток в подвздошной артерии снижается, артериальное давление практически не изменяется. На кривых кровотока и давления отчетливо видны колебания периодом 1-2 с, отражающие дыхание животного.
Результат поударной обработки этих данных представлен на рис. 10.1Б. Здесь можно видеть, что сопротивление сосудистого региона задней конечности увеличивается. Дыхательные колебания сохраняются и на среднем кровотоке, и на среднем давлении, а также хорошо выражены на кривой сопротивления.
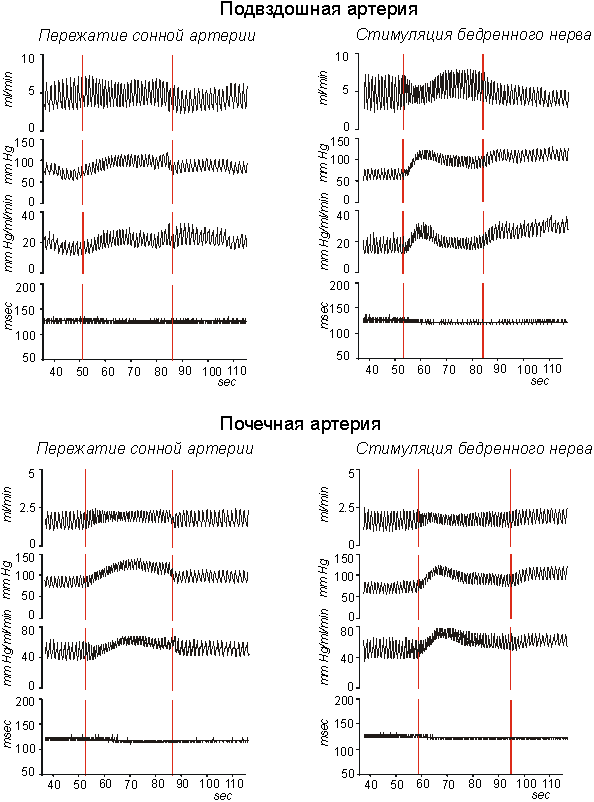
Рисунок 10.2. Изменение гемодинамических показателей в подвздошной и почечной артериях при пережатии сонной артерии и при электрическом раздражении соматических афферентов. На каждом рисунке представлены (сверху вниз): средний кровоток, среднее артериальное давление, регионарное сопротивление и пульсовой интервал.
В наших экспериментах также исследовались сосудодвигательные реакции рефлекторного происхождения. На рис. 10.2 приведены результаты поударной обработки этих экспериментов. Все кривые и на рис. 10.1, и на рис. 10.2 приведены для одной и той же крысы. Можно видеть, что сопротивление сосудистого бассейна почки выше, чем сопротивление в сосудах задней конечности. Следует также можно отметить, что изменения сопротивления исследуемого региона на пережатие сонной артерии и на стимуляцию бедренного нерва более выражены для сосудистого бассейна почки. При раздражении бедренного нерва изменение сосудистого сопротивления имеет двухфазный характер: сначала сопротивление быстро возрастает, а затем несколько снижается и устанавливается на постоянном уровне.
Заключение
Таким образом, разработанная нами методика позволяет исследовать нейрогенные ответы различных сосудистых бассейнов при воздействии на афферентные входы центральной нервной системы и при раздражении эфферентных симпатических нервов.
Описанная методика имеет несомненные преимущества перед экспериментами с изолированными сосудами и с перфузией изолированных сосудистых бассейнов. В нашей методике, во-первых, учитывается влияние гуморальных факторов, которые в организме являются вазоактивными и могут модулировать нейрогенные ответы сосудов, и содержание в крови этих факторов может изменяться при экспериментальных воздействиях.
Во вторых, в наших экспериментах поступление крови в сосудистый бассейн происходит естественным путем, без использования искусственных приспособлений (насосов). Известно, что насосы часто повреждают форменные элементы крови, что приводит к секреции из них вазоактивных факторов и, в конечном итоге – к снижению сосудистого тонуса и подавлению авторегуляции сосудов (Folkow, Borgdorff et al.).
Изучение механизмов адаптации сердечно-сосудистой системы с использованием описанной методики может включать также более детальное исследование нейрогенной регуляции сосудистых бассейнов. Методика позволяет использовать для раздражения нервов разные паттерны импульсов, имитирующие эфферентную симпатическую активность при различных функциональных состояниях организма. Это представляется важным, поскольку величина и временные характеристики сосудистого ответа существенно зависят от паттерна импульсов (Sjoblom-Widfeldt 1990). Так же, как и в опытах на изолированных сосудах (Боровик и др. 1999), разные паттерны импульсов могут задаваться программой, управляющей работой электростимулятора.
В ближайшем будущем мы собираемся применить эту методику для изучения нейрогенной регуляции сосудистого тонуса у крыс, адаптированных к условиями микрогравитации. Ранее в опытах по перфузии сосудистого бассейна задней конечности крысы физиологическим раствором мы показали, что вывешивание приводит к существенному подавлению вазоконстрикторных ответов на раздражение симпатических нервов (Machkov et al. 1997; Rodionov et al. 1999). На бодрствующих крысах нами было показано, что в отсутствие симпатических влияний у крыс сильнее проявляются негативные последствия микрогравитации (Tarasova et al., 2001). Описанная в этой статье методика позволит связать эти результаты, она может быть использована для исследования реакций не только сосудов почки и задней конечности, но и других сосудистых бассейнов, например, брыжейки и передней конечности. Сравнение сосудистых ответов разных регионов может быть крайне интересно при исследовании влияния микрогравитации на сердечно-сосудистую систему, так как недостаточное перераспределение кровотока между органами может быть одной из важных причин послеполетной ортостатической неустойчивости. Эксперименты с раздражением симпатических нервов in vivo позволят понять, как под действием микрогравитации изменяются амплитуда вазоконстрикторных ответов и их динамические характеристики при естественной перфузии кровью сосудистых бассейнов разных органов.
Исследование выполнено при поддержке Российского Фонда Фундаментальных исследований (гранты № 00-04-49276, 01-04-48932, 02-04-49193, 02-04-06652) и программы «Университеты России» (УР 11.03.004).
Литература
Study of neurogenic vasoconstrictor responses in anesthetized rat
V.O. Golubinskaya, O.S. Tarasova, A.S. Borovik, O.L. Vinogradova
Space Biomedical Center for Training and Research, Faculty of Biology, M.V.Lomonosov State University, Moscow
We developed a method to investigate neurogenic constrictor responses of hindlimb and kidney vascular beds. In anesthetized rats arterial blood pressure and blood flow velocity are measured simultaneously in artery feeding the given vascular bed. For measurements of blood flow velocity we use flowprobe 1RB connected to transit-time flowmeter Transonic Systems Inc. (Т106 model). Data recording and analysis are performed using of IBM PC and original software. The vasoconstrictor response is evaluated by the change in vascular resistance calculated as mean arterial pressure to blood flow velocity ratio. This method allows to investigate the vascular responses to vasomotor nerves stimulation and reflex changes of vascular resistance during stimulation of afferent inputs of central nervous system