Методология флоуметрии, Âûïóñê 6, 2002 ã. стр.45-68.
Комплексная оценка кровообращение в поверхностных слоях мягких тканей в различные сроки после внешнего облучения
А.В.Расулова, В.Г.Лелюк
Государственный научный центр – Институт биофизики, г. Москва
Неуклонное расширение контактов человека с источниками излучения в различных сферах его деятельности, возможность возникновения аварийных ситуаций с переоблучением участников и вовлеченных лиц, сделает актуальным дальнейшее излучение закономерностей развития и течения реакций организма на имевшее место воздействие.
Целью настоящего исследования явилась оценка с применением методов дуплексного сканирования и лазерной доплеровской флоуметрии (ЛДФ) кровообращения в поверхностных слоях мягких тканей у лиц, подвергшихся внешнему облучению в различных дозах в различные сроки наблюдения.
Материалы и методы
Обследовано 35 пациентов в возрасте от 25 до73 лет (51,07±11,5). Все исследованные были разделены на 2 группы. 1-ую группу составили 25 практически здоровых лиц в возрасте от 25 до 50 лет (средний возраст – 33,8±8,14 лет); 2-ую группу – лица, облученные в «больших» дозах, 7 мужчин в возрасте от 34 до 65 лет, перенесшие острую лучевую болезнь (ОЛБ) различной степени тяжести (доза облучения от 1,16 до 8,6 Гр) и 3 человека – 1 женщина 41 года и 2 мужчин 35 и 40 лет, подвергшихся фракционному тотальному терапевтическому облучению (ТТО) в рамках подготовки к трансплантации костного мозга (ТКМ) по поводу гемобластозов в суммарной дозе 12 Гр (2 Гр х 2 раза в сутки х 3 суток). Пациенты находились на обследовании (лечении) в Клинике ГНЦ – Института биофизики и Клинической больнице №6 ФУМБЭП при МЗ РФ по поводу различных соматических заболеваний в период с 01.10.2000 г. по 01.08.2001.
Всем больным для оценки особенностей кровообращения в коже различных участков тела, определения зависимости его характера и уровня от различных факторов, изучения реактивности субкутанных сосудов в пробах с применением различных нагрузочных тестов проводилась лазерная допплеровская флоуметрия, дуплексное сканирование с цветовым допплеровским кодированием и спектральным анализом по принятым в лаборатории клинической физиологии ГНЦ - ИБФ методикам.
ЛДФ производилась с использованием контактного накожного датчика типа «Basiс-R» диаметром 2 мм на приборе BLF 21 (Transonic Systems, США). Лазерный доплеровский флоуметр BLF 21 является измерителем капиллярного кровотока в мл/мин на 100 г ткани (средняя глубина 2 мм) капиллярной перфузии кубического миллеметра (мм3) ткани. Прибор и датчики не требовали калибровки и установки нуля. Общепринятые единицы измерения (мл/мин/100 г – миллилитров крови в минуту на 100 грамм тканей) позволяли определять абсолютное значение кровоснабжения ткани.
Обследование проводили в помещении с равномерным неярким освещением при температуре 20 – 25 Сº; исключали прием вазоактивных препаратов за 6 часов, курения - за 2 часа до момента исследования.
Изучение кровотока методом ЛДФ осуществляли в положении лежа после 10 минутного интервала. Измерения кровотока осуществляли трехкратно в симметричных точках с обеих сторон (на голове, руках, ногах, туловище) с последующим их усреднением. Общая продолжительность одного исследования составляла 2-2,5 часа.
Для изучения артериальной сосудистой реактивности субкутанных сосудов использовали функциональные нагрузочные пробы (ФНП) различной направленности (неврогенной и миогенной). Перед выполнением каждой ФНП измеряли фоновые показатели кровотока. Каждую последующую пробу проводили после возвращения кровотока к базовой величине.
Для оценки состояния неврогенного механизма регуляции сосудистого тонуса использовали температурные функциональные нагрузочные тесты - тепловой и холодовой. В качестве теплового ФНТ использовалась контактная стимуляция кожи предметом, нагретым до 40°С, в качестве холодового ФНТ - охлажденным до 10°С в течение 2 минут. Две емкости с горячей и холодной водой поочередно прикладывались к двум контралатеральным точкам, где производилось измерение.
Болевая проба проводилась в положении больного лежа на спине. Острием булавки наносились легкие уколы в различных участках тела и производилось измерение кровотока в симметричных точках. То же самое осуществлялось с противоположной стороны в точках, симметричных первоначальному измерению.
В качестве химического стимула, воздействующего на миогенный механизм ауторегуляции, применялся тест с нитроглицерином (который обладает прямым миогенным действием, способствуя быстрой вазодилятации, более выраженной в крупных артериях, с одновременным повышением сердечного выброса и снижением артериального давления). Во время проведения пробы пациенту сублингвально вводилось 0,25 мг нитроглицерина, через 2-3 минуты после чего производилась оценка субкутанного кровотока в симметричных точках тела с двух сторон.
Дуплексное сканирование выполнялось по стандартной методике «через гелевую подушку» линейным датчиком 8-15 МГц на системе Аcuson-Sequoia 512 (Аcuson, A Siemens Company, США).
Измерялись: пиковая систолическая скорость (Vps), максимальная конечная диастолическая скорость (Ved), усредненная по времени максимальная скорость (TAMX), время систолического подъема (AT), индекс периферического сопротивления (RI), пульсативный индекс (PI); время ускорения (AT), индекс ускорения (AI). Все измерения проводили в симметричных точках тела
Для обработки результатов исследования все данные были преобразованы в электронные таблицы в формате Excel. Статистический анализ проводился на IBM - совместимом персональном компьютере в пакете программ Microsoft Office' XP, Statistika 5.0, SPSS 10.0 для Windows с использованием корреляционного, вариационного, дисперсного анализов. Графические изображения построены в указанных программах.
Результаты
Результаты исследования фонового уровня кровотока в сосудах поверхностных слоев мягких тканей показывают, что у обследованных пациентов не выявлено достоверных межгрупповых отличий линейных и объемных показателей кровотока (рис. 1, 3), а также значений пульсативного индекса (рис. 2). В обеих группах значимых различий в средних величин кровотока на груди, животе, руках и бедрах выявлено не было (TAMX в 1-ой группе: на груди -2,1 см/с, на животе – 2,2 см/с, на рука – 2,4 см/с, на бедрах – 2,4 см/с, во 2-ой – 2,1 см/с, 2,2 см/с, 2,4 см/с, 2,4 м/с соответственно; PI в 1-ой – на груди - 1,2, на животе - 1,3, на руках - 1,4, на бедрах – 1,3, на спине – 1,1, во 2-ой – 1,2, 1,2,– соответственно; VF в 1-ой группе – на груди – 2,78 мл/мин/100г, на животе – 3,1 мл/мин/100г, руках – 3,5 мл/мин/100г, на бедрах – 3,2 мл/мин/100г, спине – 2,97 мл/мин/100г, во 2-ой: 2,6, 2,8, 3,3, 2,9, 2,4 м/с).
На лице, кистях рук и ягодицах отмечено достоверное повышение скоростных параметров, объемного кровотока без изменений пульсативного индекса, что вероятно связано с более высоким уровнем кровоснабжения этих участков тела в соответствии с их функциональными особенностями ( TAMX в 1-ой группе: на лице -3,6 см/с, на кистях рук – 2,9 см/с, на ягодицах – 3,1 см/с, во 2-ой – 3,5 см/с, 2,8 см/с, 2,9 см/с соответственно; PI в 1-ой – на лице - 1,78, на кистях рук - 1,7 , на ягодицах - 1,74 , во 2-ой – 1,7, 1,68, 1,74 – соответственно; VF в 1-ой группе – на лице - 5,03 мл/мин/100г, на кистях рук – 4,2 мл/мин/100г, ягодицы – 4,9 мл/мин/100г).
При расчете индексов реактивности, отражающих положительную динамику оцениваемых допплеровских параметров в ответ на функциональные нагрузочные тесты в сосудах микроциркуляторного русла в различных участках тела в группах сравнения, получены количественные параметры, представленные на рисунках 4-15.
Индексы реактивности кожного кровотока в пробе с нитроглицерином как в 1-ой, так и во 2-ой группах свидетельствовали о положительном приросте линейных (рис. 4) и объемных (рис. 6) характеристик кровотока на всех участках тела, с отрицательными значениями пульсативного индекса (рис.5). Так средние значения ИР по приросту ТАМХ составили в 1-ой группе на лице – 1,42, на груди – 1,12, на животе – 1,11, на руках – 1,13, на кисти – 1,65, на бедрах – 1,11,на спине – 1,10, на ягодицах – 1,35; во 2-ой группе – 1,38, 1,10, 1,10, 1,11, 1,62, 1,07, 1,05, 1,37 соответственно. Средние значения ИР по приросту PI в 1-ой группе на лице - 1,07, на груди - 1,05, на животе – 0,95, на руках – 1,01, на кистях – 1,08, на бедрах – 1,18, на спине – 0,94, на ягодицах – 1,04; во 2-ой группе – 0,98, 1,02, 0,93, 0,97, 1,05, 0,98, 0,94, 1,02. Средние значения ИР по приросту VF в 1-ой: 1,54, 1,27, 1,11, 1,21, 1,34, 1,27, 1,12, 1,44; во 2 – ой:1,42, 1,24, 1,10, 1,19, 1,31, 1,21, 1,11, 1,41 соответственно.
При оценке линейных скоростных характеристик кровотока мы ориентировались на изменение усредненной по времени максимальной скорости кровотока (TAMX), так как считаем, что именно этот показатель отражает наиболее достоверную информацию о потоке крови в сосуде, являясь результатом усреднения скоростных составляющих огибающей допплеровского спектра за несколько сердечных циклов.
При проведении холодовой и болевой проб у пациентов обеих групп во всех случаях отмечалась вазодилататорная реакция, характеризующаяся возрастанием скоростных параметров кровотока (рис. 7, 9 и рис.10, 12 соответственно) и снижением индексов периферического сопротивления (рис. 8 и 11 соответственно), что отражает сохранность и адекватность центральных механизмов регуляции сосудистого тонуса. Так в холодовой пробе средние значения ИР по приросту ТАМХ составили в 1-ой группе на лице – 1,24, на груди – 1,11, на животе – 1,07, на руках – 1,11, на кисти – 1,32, на бедрах – 1,10,на спине – 1,04, на ягодицах – 1,22; во 2-ой группе – 1,21, 1,10, 1,05, 1,12, 1,30, 1,10, 1,08, 1,20 соответственно. Средние значения ИР по приросту PI в 1-ой группе на лице - 1,10, на груди - 0,97, на животе – 0,90, на руках – 1,10, на кистях – 1,10, на бедрах – 0,99, на спине – 0,96, на ягодицах – 1,10; во 2-ой группе – 1,08, 0,95, 0,91, 1,05, 1,10, 0,98, 0,96, 1,10. Среднее значение ИР по приросту VF в 1-ой группе на лице – 1,42, на груди-1,22, на животе-1,11, на руках – 1,10, на кисти – 1,33, на бедрах – 1,21,на спине – 1,12, на ягодицах – 1,37; во 2-ой группе – 1,38, 1,20, 1,10, 1,08, 1,28, 1,18, 1,10, 1,34 соответственно
В болевой пробе средние значения ИР по приросту ТАМХ составили в 1-ой группе на лице – 1,28, на груди – 1,14, на животе – 1,10, на руках – 1,11, на кисти – 1,25, на бедрах – 1,12,на спине – 1,12, на ягодицах – 1,31; во 2-ой группе – 1,27, 1,13, 1,08, 1,12, 1,23, 1,11, 1,14, 1,34 соответственно. Средние значения ИР по приросту PI в 1-ой группе на лице - 1,10, на груди - 1,08, на животе – 0,97, на руках – 0,90, на кистях – 1,10, на бедрах – 1,05, на спине – 0,90, на ягодицах – 1,10; во 2-ой группе – 1,11, 1,06, 0,95, 0,91, 1,07, 1,03, 0,93, 1,10. Средние значения ИР по приросту VF в 1-ой: 1,35, 1,27, 1,11, 1,12, 1,29, 1,14, 1,11, 1,32; во 2 – ой:1,31, 1,21, 1,08, 1,11, 1,27, 1,11, 1,09, 1,30 соответственно.
В тепловой пробе линейные и объемные скоростные показатели (рис. 13, 15), а так же значения индекса пульсации (рис. 14) в группах сравнения практически не менялись. Наличие отрицательных реакций у обследуемых пациентов несомненно связано с существованием зависимости между наличием и степенью выраженности сосудистого ответа и индивидуальным порогом температурной чувствительности. В тепловой пробе средние значения ИР по приросту ТАМХ составили в 1-ой группе на лице – 1,28, на груди – 1,14, на животе – 1,10, на руках – 1,11, на кисти – 1,29, на бедрах – 1,11,на спине – 1,09, на ягодицах – 1,28; во 2-ой группе – 1,30, 1,12, 1,11, 1,10, 1,27, 1,13, 1,10, 1,31 соответственно. Средние значения ИР по приросту PI в 1-ой группе на лице - 1,11, на груди - 1,07, на животе – 0,92, на руках – 1,04, на кистях – 1,10, на бедрах – 1,02, на спине – 0,97, на ягодицах – 1,10; во 2-ой группе – 1,10, 1,05, 0,94, 1,02, 1,10, 1,10, 0,95, 1,10. Средние значения ИР по приросту VF в 1-ой: 1,31, 1,21, 1,11, 1,18, 1,29, 0,99, 1,11, 1,25; во 2 – ой:1,28, 1,20, 1,10, 1,15, 1,27, 1,10, 1,10, 1,22 соответственно.
Таким образом, из представленных данных следует, что значимых различий как фоновых параметров субкутанного кровотока в сосудах микроциркуляторного русла, так и различий в значениях индексов реативности, отображающих положительную динамику показателей кровотока на миогенный и неврогенный стимулы не выявлено.
Обсуждения результатов
Из систематизированного клинического материала [1,2,4,7], характеризующего лучевую болезнь и ее последствия у людей пострадавших во время атомного взрыва, при авариях с источниками ионизирующих излучений, нарушения техники радиационной безопасности или подвергшихся общему облучению в терапевтических целях, хорошо известно, что у таких лиц обнаруживается целый комплекс «остаточных изменений», указывающих на неустойчивость регуляторных систем организма, отсутствие полноценной репарации предшествующих тканевых и системных нарушений. Гистологическое исследование обнаруживает многообразную картину поражения капилляров и артериол во внутренних органах, снижение периферической циркуляции. Так, по некоторым данным после облучения развивались восходящее поражение артерий, перикапиллярный гиалиноз, запустевание крупных артерий с диффузным утолщением интимы и меди типа облитерирующего тромбангиита [3,4,8].
В случае более тяжелого поражения, когда патология сосудов приобретает характер органических повреждений, выявляются нарушения сосудистых проб, свидетельствующие о повышенной хрупкости капилляров [9,10]. Отмечается неустойчивость кожно-сосудистых реакций, нарушение терморегуляции, падение сосудистого тонуса со снижением артериального давления, усиление проницаемости капилляров [1,2,12].
О характере структурных изменений сосудов можно судить по результатам динамических капилляроскопических наблюдений [2,11,13]. Ход артериальных и венозных ветвей в области ногтевого ложа, слизистой губ, языка, щек, в конъюнктиве оказывается неправильным, капилляры изогнуты, образуют клубки, местами резко расширены, или сужены, или закрыты полностью. Обнаружены также раскрытые артериовенозные анастомозы, выключающие целые зоны капиллярной сети из кровотока. В поздние сроки после перенесенной лучевой болезни снижается или извращается реактивность сосудов при воздействии различных агентов [9,10,13].
Анализ данных, полученных нами при сравнении уровня фонового субкутанного кровотока, не выявил значимых различий в исследуемых группах. Полученные как 1-ой, так и во 2-ой группах зональные отличия были обусловлены характерными особенностями строения микрососудистого русла в точках исследования, а именно различной частотой пространственного расположения капилляров, интенсивностью микроциркуляции и наличием артериоло-венулярных анастомозов. В функционально активных участках кожи плотность капиллярной сети больше, а так же велико количество атрериоло-венулярных шунтов, что обусловливает увеличение интенсивности кровотока на микроциркулярном уровне. Таким образом, более высокая васкуляризация соответствует активным в функциональном отношении участкам кожи [5,16]. Несмотря на наличие номинальной разницы значений показателей кровотока, достоверных отличий выявлено не было. Так у облученных пациентов фоново не зафиксировано изменений периферической циркуляции.
Для оценки вазодилататорной способности сосудистого русла использовалась ФНП с нитроглицерином, воздействующим на миогенный механизм ауторегуляции. Из различных источников известно, что механизм действия данного препарата двоякий: как местный – на стенки сосудов, так и центральный – посредством сосудодвигательных центров. Нитроглицерин считается наиболее сильным вазодилятатором, действующим посредством угнетения сосудодвигательных центров, что было неоднократно подтверждено в различных экспериментах и клинических наблюдениях [5,20,21].
Нарушение вазодилятаторной способности сосудистой стенки может быть обусловлено влиянием различных факторов: общесоматических, а также ионизирующим излучением. Так многие авторы считают, что воздействие больших доз ионизирующего излучения приводит к фиброзно-склеротическим изменениям в сосудистом русле, в результате чего происходит нарушение вазодилятаторной способности сосудов МЦР на действие прямых миогенных стимулов [5,6,24,25]. Кроме того, нельзя игнорировать влияния на функции миогенного механизма локальной сосудистой регуляции сопутствующих системных сосудистых процессов[13,14,16,18,19].
Анализируя характер изменения параметров кровотока сосудов МЦР после введения 0,25 мг нитроглицерина сублингвально, разница в значения скоростных и объемных показателей сосудистого русла между пациентами 2 группы и группой контроля не выявлена, что доказывает отсутствие функционально значимого поражения сосудов микрорусла в отдаленном периоде после облучения.
Для изучения состояния неврогенной регуляции сосудистого тонуса в проведенном исследовании использовались температурные (тепловая и холодовая) и болевые функциональные нагрузочные пробы.
Боль возникает при раздражении чувствительных нервных окончаний, заложенных в коже, мышцах, сосудах. Возбуждение от них передается в центральную нервную систему по нервным волокнам. В эксперименте в ответ на легкие раздражения вначале следует расширение, как артерий, так и капилляров. Ток крови ускоряется. При усилении раздражения начальное расширение сменяется кратковременным сужением, а затем , при еще более острых и длительных местных воздействиях, наступает уже паралитическое расширение – сперва одних лишь капилляров, а затем и артерий. В этой стадии адреналин (при местном применении) не оказывает на сосудистый тонус никакого эффекта – тонус парализован; ток крови сильно замедляется, почти до стаза. [6].
При проведении болевой проб у пациентов обеих групп во всех случаях отмечалась вазодилататорная реакция, что отражает сохранность и адекватность центральных механизмов регуляции сосудистого тонуса.
Температурные пробы позволяют оценить возможность сосудов микроциркуляторного русла к осуществлению своих основных функций - изменению просвета (спазм, расширение). При местном нагревании кожи возникает расширение сосудов, являющееся в первую очередь результатом ослабления тонуса сосудов вследствие центральных рефлексов, а не прямого воздействия на кровеносные сосуды. Эти рефлексы осуществляются на уровне гипоталамических центров терморегуляции и реализуются через симпатические сосудосуживающие нервы. Резкое холодовое раздражение кожи может вызвать кратковременное расширение сосудов, которое может не зависеть от нервных влияний [6,12,16,24,25].
У лиц как 1-ой так и 2-ой групп сосудистый ответ на предъявление теплового и холодового нагрузочных стимулов приводил к приблизительно одинаковой по выраженности вазодилататорной реакции, чуть более выраженной на холодовой раздражитель, направленной на обеспечение постоянства локального гомеостаза.
Вывод
Проведенная нами комплексная оценка кровообращения в поверхностных слоях мягких тканей в различные сроки после внешнего облучения показала, что в отдаленном периоде наблюдения у пациентов, перенесшие острую лучевую болезнь различной степени тяжести (в результате внешнего облучения в дозах от 1,16 до 8,6 Гр), а также подвергшиеся тотальному терапевтическому облучению (в суммарной дозе 12 Гр), не выявлено значимых различий величин фоновых параметров кровотока, а также сосудистой реактивности в микрорусле.
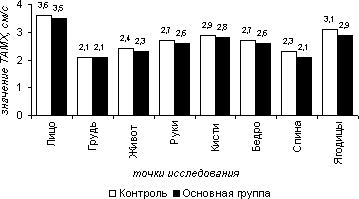
Рисунок 5.1. Фоновые значения усредненной по времени максимальной скорости кровотока (TAMX) в группах сравнения
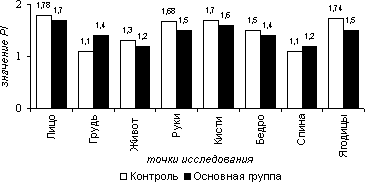
Рисунок 5.2. Фоновые значения индекса пульсации (PI) в группах сравнения
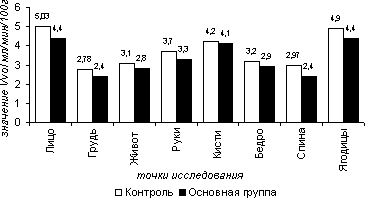
Рисунок 5.3. Фоновые значения объемной скорости кровотока (Vvol) в группах сравнения
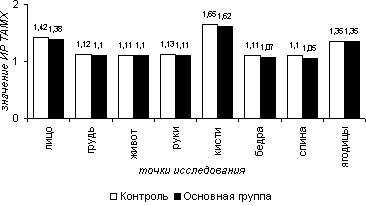
Рисунок 5.4. Индекс реактивности (ИР) усредненной по времени максимальной скорости кровотока (TAMX) в нитроглицериновой пробе в различных участках тела в группах сравнения
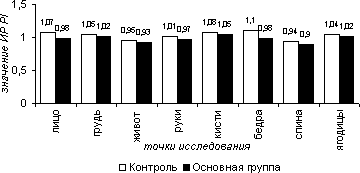
Рисунок 5.5. Индекс реактивности (ИР) индекса пульсации (PI) в нитроглицериновой пробе в различных участках тела в группах сравнения
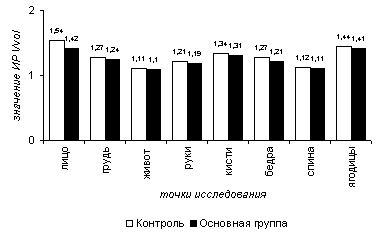
Рисунок 5.6. Индекс реактивности (ИР) объемной скорости кровотока (Vvol) в нитроглицериновой пробе в различных участках тела в группах сравнения
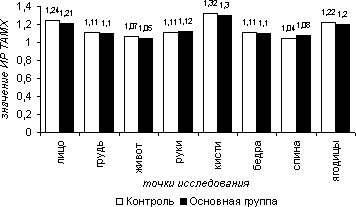
Рисунок 5.7. Индекс реактивности (ИР) усредненой по времени максимальной скорости кровотока (TAMX) в холодовой пробе в различных участках тела в группах сравнения
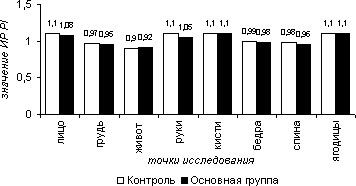
Рисунок 5.8. Индекс реактивности (ИР) индекса пульсации (PI) в холодовой пробе в различных участках тела в группах сравнения
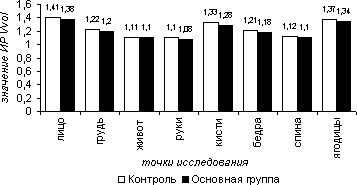
Рисунок 5.9. Индекс реактивности (ИР) объемной скорости кровотока (Vvol) в холодовой пробе в различных участках тела в группах сравнения
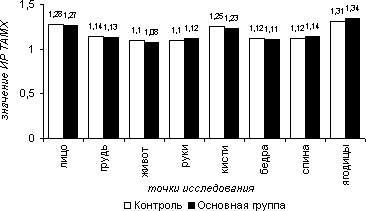
Рисунок 5.10. Индекс реактивности (ИР) усредненной по времени максимальной скорости кровотока (TAMX) в болевой пробе в различных участках тела в группах сравнения
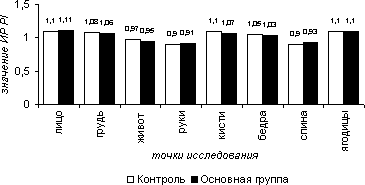
Рисунок 5.11. Индекс реактивности (ИР) пульсативного индекса (PI) в болевой пробе в различных участках тела в группах сравнения
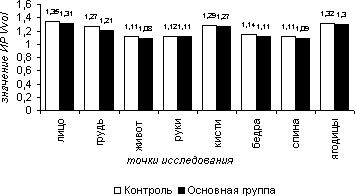
Рисунок 5.12. Индекс реактивности (ИР) объемной скорости кровотока (Vvol) в болевой пробе в различных участках тела в группах сравнения
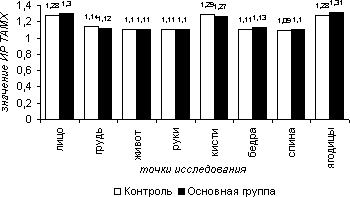
Рисунок 5.13. Индекс реактивности (ИР) усредненной по времени максимальной скорости кровотока (TAMX) в тепловой пробе в различных участках тела в группах сравнения
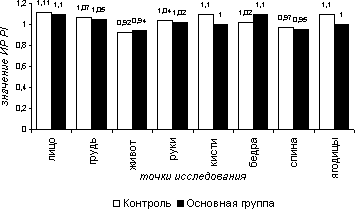
Рисунок 5.14. Индекс реактивности (ИР) пульсативного индекса (PI) в тепловой пробе в различных участках тела в группах сравнения
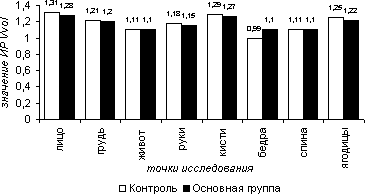
Рисунок 5.15. Индекс реактивности (ИР) объемной скорости кровотока (Vvol) в тепловой пробе в различных участках тела в группах сравнения
Список литературы
Complex valuation of microcirculation in tissue surface in various periods after exposure
A.V.Rasulova, V.G.Leluk
Russian Stae Research Centre – Institute of Biophysics, Moscow, Russia